Benötigen Nahrungsergänzungsmittel eine behördliche Zulassung?

Nahrungsergänzungsmittel sollen dem Körper besondere ernährungsphysiologische Wirkungen verleihen und liegen bei Verbrauchern hoch im Trend. Da Nahrungsergänzungsmittel jedoch Lebensmitteln sind, gibt es in rechtlicher Hinsicht viel zu beachten. Wir klären, ob Nahrungsergänzungsmittel vor dem erstmaligen Vertrieb einer behördlichen Zulassung bedürfen.
Inhaltsverzeichnis
Grundsatz: Nur Anzeigepflicht
Nahrungsergänzungsmittel sind, anders als etwa Arzneimittel, grundsätzlich nicht zulassungspflichtig.
Ihr Inverkehrbringen in Deutschland muss allerdings angezeigt werden. Dies ergibt sich aus § 5 der Nahrungsergänzungsmittelverordnung (NemV).
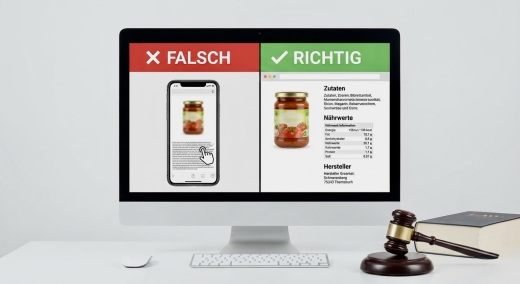
Danach sind Hersteller oder Einführer, welche ein Nahrungsergänzungsmittel auf dem Markt der Bundesrepublik Deutschland erstmalig bereitstellen, verpflichtet, dies spätestens im Zeitpunkt des ersten Angebots dem Bundesamt für Verbraucherschutz und Lebensmittelsicherheit unter Vorlage eines Musteretiketts für das Erzeugnis anzuzeigen.
Diese Anzeigepflicht gilt nur, wenn ein Nahrungsergänzungsmittel erstmalig aus einem anderen Land auf dem deutschen Markt bereitgestellt werden soll. Betroffen von der Pflicht sind insofern Hersteller oder Importeure (auch Händler), die Nahrungsergänzungsmittel aus anderen Ländern beziehen. Für bereits auf dem deutschen Markt zirkulierende Mittel gilt die Anzeigepflicht nicht.
Die Anzeigepflicht gilt nicht nur bei erstmaliger Einfuhr von Nahrungsergänzungsmitteln aus Drittländern, sondern auch bei solchen aus anderen EU-Mitgliedsstaaten. Eine EU-weit gültige Anzeige gibt es gerade nicht.
Somit gilt auch, dass bei einer Bereitstellung auf dem Markt eines anderen EU-Landes grundsätzlich auch bei der dort zuständigen Behörde eine Anzeige getätigt werden muss.
Wurde ein Nahrungsergänzungsmittel schließlich vor der Marktbereitstellung in Deutschland schon in einem anderen EU-Mitgliedsstaat in Verkehr gebracht, muss die Anzeige nach § 5 NemV unbedingt auch die Behörde dieses Mitgliedsstaats benennen.
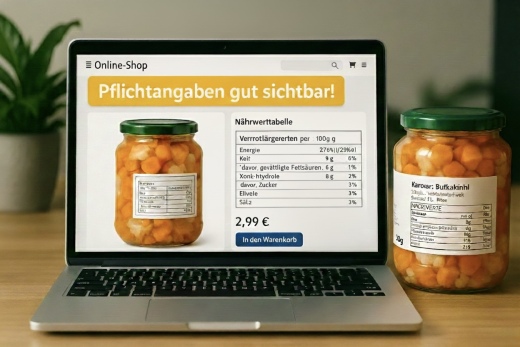
Beim Verkauf von Nahrungsergänzungsmittel sind diverse weitere kennzeichnungsrechtliche und melderechtliche Pflichten zu beachten.
Die Voraussetzungen für einen rechtssicheren Nahrungsergänzungsmittel-Verkauf hat die IT-Recht Kanzlei in diesen FAQ zusammengetragen.
Ausnahme: Novel Foods
Eine Ausnahme von der bloßen Anzeigepflicht für Nahrungsergänzungsmittel existiert für sog. neuartige Lebensmittel („Novel Foods“).
Darunter versteht man alle Lebensmittel, die vor dem 15. Mai 1997 nicht in nennenswertem Umfang in der Europäischen Union für den menschlichen Verzehr verwendet wurden und die in mindestens eine der in Artikel 3 der Novel Food-Verordnung (EU) genannten Kategorien fallen.
Hierzu zählen Lebensmittel
- mit neuer oder gezielt veränderter Molekularstruktur
- aus Mikroorganismen, Pilzen oder Algen
- aus Materialien mineralischen Ursprungs
- aus Pflanzen oder Pflanzenteilen
- aus Tieren oder deren Teilen
- aus Zell- oder Gewebekulturen
- die durch ein neuartiges, nicht übliches Verfahren hergestellt wurden
- aus technisch hergestellten Nanomaterialien
- die Vitamine, Mineralstoffe und andere Stoffe sind
Für Nahrungsergänzungsmittel, die als „Novel Foods“ gelten, ist beim erstmaligen Inverkehrbringen in der EU eine vorherige Zulassung auf EU-Ebene erforderlich.
Zulassungspflichtig sind alle Novel Foods, die noch nicht in die von der EU geführten Positivliste zugelassener neuartiger Lebensmittel aufgenommen sind.
Über die Zulassung entscheidet die EU-Kommission. Dafür muss bei dieser ein Antrag auf Zulassung mit vollständiger Dokumentation des Erzeugnisses eingereicht werden. Über die Anträge befindet die EU-Kommission zusammen mit den Mitgliedsstaaten unter Einbeziehung der Europäischen Behörde für Lebensmittelsicherheit (EFSA).
Eine Zulassung steht unter anderem noch aus für:
- synthetisches Cannabidiol
- Koriandersamenöl
- Kurkumaextrakt
- Mungobohnenprotein
- Wasserlinsenpulver
Fazit
Sollen Nahrungsergänzungsmittel erstmalig in Deutschland in Verkehr gebracht werden, ist hierfür grundsätzlich keine Zulassung, sondern nur eine Anzeige erforderlich.
Eine Zulassungspflicht auf EU-Ebene gilt aber für Nahrungsergänzungsmittel, die als neuartige Lebensmittel gelten und daher ein besonderes gesundheitliches Risikopotenzial begründen.
Fragen zum Beitrag? Diskutieren Sie hierzu gerne mit uns in der Unternehmergruppe der IT-Recht Kanzlei auf Facebook.
Link kopieren
Als PDF exportieren
Per E-Mail verschicken
Zum Facebook-Account der Kanzlei
Zum Instagram-Account der Kanzlei



0 Kommentare